電界撹拌技術の開発
先進プロセス開発部 中村 竜太
大久保 義真
久住 孝幸
企画事業部 赤上 陽一
技術の背景
近年、精密加工技術を医療技術に応用する動きが高まっています。その中で、μLオーダーの微小液滴に対する撹拌技術が注目されています。液量を減らすことによって、被撹拌物質同士の移動距離が短くなり、反応の向上が期待されます。また、微少量にすることによって、溶液のランニングコストや廃液を低減することができます。さらに、医療検査への応用においては、被検者から採取するサンプル量を微量化することによって、低侵襲な検査を実現できます。しかしながら、一般的に、微少量液滴は撹拌が困難であると言われています。攪拌挙動は液滴が接する底界面の面積に依存し、面積が小さい微少量液滴は乱流を生成しづらくなることが理由です。
微少量液滴の撹拌技術として、ナノサイズの撹拌子による撹拌や超音波による撹拌の報告はされていますが、それぞれコンタミネーションによる汚染や超音波振動子に起因する液温上昇によるタンパク質・細胞等の熱変性を招く懸念があるとされています。
我々は、以前から、スラリーに外部から電界を与えて、配置制御を生じさせる電界砥粒制御技術を開発してきており、既に県内企業とともに工具刃先の仕上げ加工の開発・事業化や研磨技術の高効率化等の研究開発・応用を行っております。さらには、この電界砥粒制御技術を発展させ、微小液滴に電界を与えることで、介在物を用いずに、非接触で撹拌を可能にする革新的な撹拌技術、”電界撹拌技術”を開発しています。今回はその技術を紹介いたします。
電界撹拌技術について
|
|
|
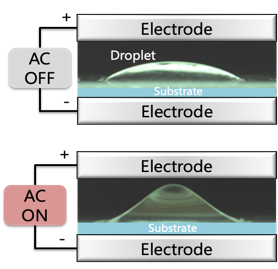
図1 電界撹拌の様子 |
電界撹拌は当センター独自の技術です。具体的には、平行平板間に滴下された液滴に高電圧電界を非接触環境下で印加することで吸引力を発生させ、液滴の挙動を制御し、その内部の被撹拌物質を運動させて撹拌させる技術です。電界撹拌の挙動写真を図1に示します。電場を印加すると液滴に吸引力が作用し、上電極側に吸引、電場の変化により液滴は上下に運動する様子が見てとれます。
また、液滴内部の撹拌挙動を図2に示します。液量は20μLで、超純水の中にナノビーズを沈降させています。交流電場を与えた直後に撹拌現象が生じていることが観察できます。
|
|
|
図2 電界撹拌時の液滴内部の様子 |
|
|
|
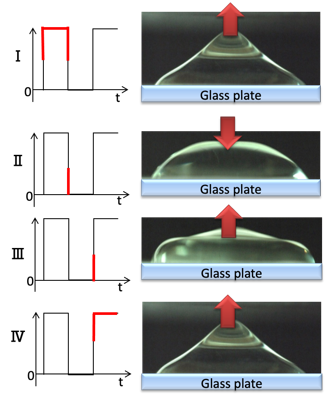
図3 印加波形に対応する撹拌挙動 |
次に、印加電界波形に対応する撹拌挙動を図3に示します。印加する矩形波の赤色部分に対応する液滴の状態を右図に示しています。電界ONで吸引力が液滴に発生し、電極に引っ張られます(Ⅰ)。次にOFFにすると吸引力は無くなり、液滴先端は下降します(Ⅱ)。次に降下した液滴はガラス基板に当たる反発力によって、液滴は再び上昇します(Ⅲ)。上昇中の液滴に再度電界をONにすると、電極側に吸引されます(Ⅳ)。このように、本技術は従来の振とう撹拌の様な平面的2次元撹拌ではなく、3次元的な撹拌を創出可能です。そして、本撹拌技術はスターラー等を用いないコンタミレスな撹拌方法です。また、本撹拌技術は室温で使用する限り、タンパク質や組織の変性や熱的な細胞侵襲の恐れが非常に少ないという大きな特徴があります。
医療分野(手術中のがん迅速診断)への応用
|
|
|
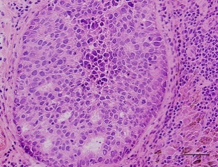
図4 肺がんリンパ節のHE染色像 |
近年、がん治療は進行度や悪性度に応じた個別化治療を行う傾向にあり、その一つである手術中の病理診断は個別化の判断根拠として重要です。現状、HE(ヘマトキシリン・エオジン)染色が行われています。HE染色した肺がんリンパ節転移写真を図4に示します。病理医は、この方法を用いて染色した組織中の細胞の核内構造や細胞形態を観察して診断していますが、HE染色の診断には限界があるとされ、2mm以下とされる微小な転移を見逃す可能性が指摘されています。この微小転移を見逃さずに診断するためには免疫組織染色(以下、免疫染色)が有効です。しかしながら、従来の免疫染色法は、生体組織が載せられたスライドガラスに抗体液を滴下後、静置状態にて抗原抗体反応を行っています。この反応ではブラウン運動(液体・気体中の微粒子が、さまざまな方向に、不規則に動き回る現象)に支配されて、反応に長時間を要してしまいます。それ故に手術中の病理診断には適用できないという課題がありました。
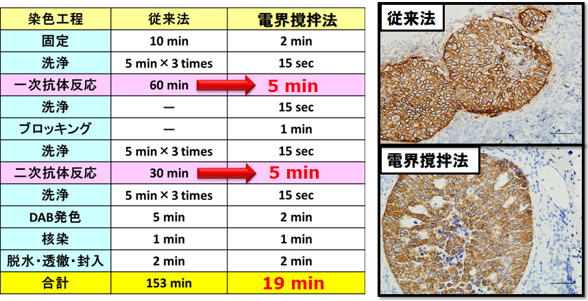
そこで、当センターで開発した電界撹拌技術を免疫染色の抗原抗体反応工程に導入することで、従来約2時間以上費やしていた時間を20分程度まで迅速化することができ、手術中の迅速免疫染色を可能としました。従来静置法と電界撹拌法の染色プロトコール比較表と実際の免疫染色写真を図5に示します。このように20分程度で従来法と同等な染色品位を得られたました。また、染色時間の短縮化とともに高価な抗体濃度の低減も可能になることを明らかにしました。何より微小転移の検出確度が高まることで、手術中の診断精度が向上すること、抗体種によっては、がんの性状が明らかになり、原発性、転移性の判定も明らかにしました。また、従来まで、手術中の確定診断結果と術後の診断結果との差異が生じる場合、再度手術が必要になる症例が特に脳腫瘍で存在しています。本迅速染色法を導入することで、手術手法や治療方法の最適な指示がなされ、よって、患者の予後のQOL向上や医療費削減が可能となります。
|
|
|
図5 免疫染色のプロトコール |
|
|
|
図6 電界撹拌染色装置R-IHC ラピート |
これらは秋田大学医学部をはじめ、県内企業と連携し、精密加工技術と医療技術の融合、さらに研究会による人と人との出会いを通じて、医療ニーズであった手術中の迅速な免疫染色に、当センター独自の技術である電界撹拌技術を適応することによって可能にすることができました。装置開発並びに製造は秋田エプソン株式会社が担い2014年5月12日にヒストテック®R-IHC®(愛称:ラピート)としてサクラファインテックジャパン株式会社から上市されています。薬機法分類は一般医療機器(クラスⅠ)で製造販売届出番号13B3X00052014001です。実際に上市された電界撹拌染色装置を図6に示します。
今後の展望
本診断支援装置を用いた臨床応用として、既に秋田大学病院関係に導入され約1000例の実績があります。電界撹拌技術を用いた迅速免疫染色法を実施することにより、微小転移の検出感度向上により手術中の診断精度が向上、さらに高価な抗体濃度の大幅な削減も可能となります。これまでは、2度手術が必要になる症例が一度の手術で済むことから、医師及び患者の負担が大幅に低減される等、メディカルイノベーションが期待されています。
現在、本装置の自動化を目指しており、秋田エプソン株式会社、秋田大学医学部と連携して開発を行っています。さらに、今後、本装置をベースとした遠隔診断支援、さらにはAI病理診断等を通じたDX(デジタルトランスフォーメーション)の推進にも寄与できればと考えています。
撹拌技術はまさに基盤技術であり、医療検査分野においてDNA検査、酵素免疫測定法への応用にも着手しております。2020年初頭から、現在に至るまでも世界的に猛威を振るっているCOVID-19 (新型コロナウイルス感染症) は、SARS-CoV-2ウイルスによって引き起こされる感染性の高い呼吸器疾患です。2021年6月14日現在までに、世界で確認された感染者数は約1億8千万人、死亡者数は約380万人に達しています。COVID-19の主な検査は、現在感染しているかを調べるPCR検査と抗原検査、過去に感染したかを調べる抗体検査であり、それぞれのステージや症状に応じて適切な検査が行われています。これらの検査に、電界撹拌技術を用いる研究開発を現在行っています。迅速かつ高感度な検査システムを構築し、CIVID-19をはじめ、インフルエンザ、風疹等様々な検査へ応用可能な秋田発の技術で社会的貢献ができればと考えています。